Воспалительное заболевание кишечника. Генетика
Воспалительное заболевание кишечника
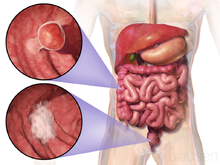
Люди с воспалительным заболеванием кишечника ( язвенный колит и болезнь Крона ) подвергаются повышенному риску рака толстой кишки. Риск увеличивается, чем дольше человек заболевает, и тем хуже степень воспаления. В этих группах высокого риска рекомендуется как профилактика аспирином, так и регулярная колоноскопия . Эндоскопическое наблюдение в этой группе высокого риска может снизить развитие колоректального рака путем ранней диагностики, а также может снизить вероятность смерти от рака толстой кишки. Люди с воспалительным заболеванием кишечника составляют менее 2% случаев рака толстой кишки в год. У людей с болезнью Крона 2% заболевают колоректальным раком через 10 лет, 8% через 20 лет и 18% через 30 лет. У людей, страдающих язвенным колитом, примерно у 16% развивается предшественник рака или рак толстой кишки в течение 30 лет.
Генетика
Те, у кого семейный анамнез есть у двух или более родственников первой степени (например, один из родителей или брат или сестра), имеют в два-три раза больший риск заболевания, и на эту группу приходится около 20% всех случаев. Ряд генетических синдромов также связан с более высокими показателями колоректального рака. Наиболее распространенным из них является наследственный неполипозный колоректальный рак (HNPCC или синдром Линча), который встречается примерно у 3% людей с колоректальным раком. Другие синдромы, которые тесно связаны с колоректальным раком, включают синдром Гарднера и семейный аденоматозный полипоз (FAP). У людей с этими синдромами рак почти всегда возникает и составляет 1% случаев рака. Тотальная проктоколэктомия может быть рекомендована людям с ФАП в качестве профилактической меры из-за высокого риска развития злокачественных новообразований. Колэктомия, удаление толстой кишки, может быть недостаточной профилактической мерой из-за высокого риска рака прямой кишки, если прямая кишка остается.
Мутации в паре генов ( POLE и POLD1 ) были связаны с семейным раком толстой кишки.
Большинство смертей от рака толстой кишки связаны с метастазированием. Ген, который, по-видимому, вносит вклад в потенциал метастазирования, метастазирование, связанное с раком толстой кишки 1 ( MACC1 ). Это транскрипционный фактор, который влияет на экспрессию фактора роста гепатоцитов . Этот ген связан с пролиферацией, инвазией и рассеянием раковых клеток толстой кишки в клеточной культуре, а также с ростом опухоли и метастазированием у мышей. MACC1 может быть потенциальной мишенью для лечения рака, но эта возможность должна быть подтверждена клиническими исследованиями.
Эпигенетические факторы, такие как аномальное метилирование ДНК промоторов, подавляющих опухоль, играют роль в развитии колоректального рака.
У евреев-ашкенази риск заболеть аденомами, а затем и раком толстой кишки на 6% выше, поскольку ген APC встречается чаще.












 Круговая диаграмма, показывающая частоту немелкоклеточного рака легкого по сравнению с мелкоклеточным раком, показанным справа, с долями курящих и некурящих, показанными для каждого типа.
Круговая диаграмма, показывающая частоту немелкоклеточного рака легкого по сравнению с мелкоклеточным раком, показанным справа, с долями курящих и некурящих, показанными для каждого типа. 

